Образование карбоновых кислот. Физические и химические свойства карбоновых кислот. Уксуснокислое брожение этанола
Тема: Карбоновые кислоты
План лекции:
- Понятие о карбоновых кислотах.
- Гомологический ряд карбоновых кислот.
- Одноосновные предельные карбоновые кислоты.
- Изомерия и номенклатура.
- Нахождение в природе.
- Физические и химические свойства карбоновых кислот.
Карбоновые кислоты очень распространены в быту и промышленности. Уксусная кислота – одна из первых кислот, которая была известна человеку. Уже в древние времена она была выделена из уксуса, а последний получался при скисании вина.
С карбоновыми кислотами мы уже встречались при изучении химических свойств альдегидов. В молекулах карбоновых кислот содержится характерная группировка атомов – карбоксильная группа.
Карбоновые кислоты – это органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединенных с углеводородным радикалом или водородным атомом.
Карбоновые кислоты классифицируют: а) в зависимости от числа карбоксильных групп в молекуле на одноосновные, двухосновные и многоосновные; б) в зависимости от природы радикала на предельные, непредельные и ароматические.
Одноосновные предельные карбоновые кислоты. Одноосновным предельным карбоновым кислотам можно дать такое определение:
К основным предельным карбоновым кислотам относятся органические вещества, в молекулах которых имеется одна карбоксильная группа, связанная с радикалом предельного углеводорода или с атомами водорода.
Строение молекул карбоновых кислот можно установить теми же методами, которые были рассмотрены при изучении альдегидов.
Атом водорода в гидроксильной группе карбоновых кислот гораздо более подвижен, чем в молекулах спиртов. Поэтому растворимые в воде карбоновые кислоты отщепляют ионы водорода и окрашивают лакмус в красный цвет:
RCOOH ↔ RCOO - + H +
Изомерия и номенклатура. Изомерия предельных одноосновных карбоновых кислот аналогична изомерии альдегидов.
Чаще всего употребляются исторически сложившиеся названия кислот (муравьиная, уксусная и т.д.). По международной номенклатуре их образуют от названия соответствующих углеродов с прибавлением окончания –овая и слова «кислота», например: метановая кислота .
Нахождение в природе
Муравьиная кислота содержится в муравьях, в крапиве и хвое ели. Ожог крапивой – результат действия муравьиной кислоты. Масляная (бутановая) кислота входит прогорклого масла, а валериановая (пентановая) кислота содержится в корнях валерианы.
Получение
В лаборатории карбоновые кислоты, как и не органические, можно получить из их солей, действуя на них серной кислотой при нагревании:
2CH 3 COONa + H 2 SO 4 → Na 2 SO 4 + 2CH 3 COOH
Физические свойства
Низшие карбоновые кислоты – жидкости с острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной массы растворимость кислот в воде уменьшается, а температура кипения повышается. Высшие кислоты начиная с пеларгоновой (ионановой) CH 3 –(CH 2) 7 –COOH, – твердые вещества, без запаха, нерастворимые в воде.
Химические свойства.
Общие свойства карбоновых кислот аналогичны соответствующим свойствам неорганических кислот.
Карбоновые кислоты обладают и некоторыми специфическими свойствами, обусловленными наличием в их молекулах радикалов. Так, например, уксусная кислота реагирует с хлором:
Cl 2 + CH 3 COOH → ClCH 2 COOH + HCl
Муравьиная кислота по химическим свойствам от других карбоновых кислот.
1. Из одноосновных кислот муравьиная является самой сильной кислотой.
2. Из-за особенности строения молекул муравьиная кислота подобно альдегидам легко окисляется (реакция серебряного зеркала):
HCOOH + Ag 2 O → HOCOOH + 2Ag↓
HOCOOH ↔ H 2 O + CO 2
3. При нагревании с концентрированной серной кислотой муравьиная кислота отщепляет воду и образуется оксид углерода (II):
HCOOH → H 2 O + CO
Эта реакция используется для получения оксида углерода (II) в лаборатории.
Карбоновые кислоты. Непредельные (ненасыщенные) карбоновые кислоты - соединения, в углеводородном радикале которых имеются кратные связи. В зависимости от их числа и природы различают: 1) алкеновые карболовые кислоты с общей формулой C*H2*-iCOOH, имеющие одну двойную связь; 2) алкадиеновые карбоновые кислоты с общей формулой СяНгя-зСООН, имеющие две двойные связи; 3) алкатриеновые карбоновые кислоты с общей формулой СяНгл-зСООН, имеющие три двойные связи; 4) алкиновые карбоновые кислоты с общей формулой ОД^-эСООН, имеющие одну тройную связь. Способ получения. 1. Окисление непредельных альдегидов: акролеин акриловая кислота 2. Дегидрогалогенирование галогенкарбоновых кислот: СН2-СН2-СН2-СООН + 2КОН - сн2=сн-сн2-соок+2И2о+ка 3. Дегидратация р-оксикислот: Физические свойства. Ненасыщенные карбоновые кислоты с числом атомов углерода 10 и более, имеющие ^^-конфигурацию, в отличие от предельных карбоновых кислот при обычных условиях являются жидкостями. 7/?а«оизомеры непредельных карбоновых кислот с любым числом атомов углерода являются кристаллическими веществами. . В табл. 29.3 указаны физические свойства некоторых представителей непредельных карбоновых кислот. Таблица 29.3. Физические свойства некоторых представителей непредельных карбоновых кислот Название кислоты Формула Температура плавления, °С Температура дпвниж, °С Акриловая С2Н3-СООН 12,1 140,9 Пропиоловая С2Н - СООН 17,6 144 Кро тоновая (тране- из ом ер) С3Н5-СООН 71,4-71,7 185 Название кислоты Формул» Температура плавления, °С Температура X) Изокро тоновая (tfuc- изомер) С3Н5-СООН 15,5 169 Олеиновая (цис-изомер) С17Н33СООН 13,4 228/15 Эландиновая (транс-изомер) С17Н33СООН 44 234/15 Линолевая Ci7H3iCOOH -5 149Д Линоленовая C,7H29COOH -11,3 184/4 Последние четыре кислоты кипят при низких давлениях (указаны в мм рт. ст. через дробь). Химические свойства. Наличие в углеводородном радикале двойных и тройных связей влияет на силу карбоновых кислот. Если у пропионовой кислоты константа диссоциации К- = 1,34 Ю, то у акриловой кислоты она приблизительно в 4 раза больше (#=5,6* 10"5), а у пропиоловой кислоты она больше в тысячу раз (К= 1,35 ИГ1). Наличие кратных связей в молекулах непредельных карбоновых кислот обусловливает их способность вступать в реакции присоединения и полимеризации и особенности протекания реакций окисления. 1. Реакции присоединения: 2. Реакции полимеризации: соон соон 3. Реакции окисления: а) при осторожном окислении образуются диоксикислоты акриловая диоксипропноновая кислота кислота б) при энергичном окислении происходит разрыв молекулы по месту кратной связи с образованием смеси одноосновной и двухосновной кислот: СНз-СН«СН-СООН гротоповая кислота СН эСООН+НООС - СООН уксусная щавелевая кислота кислота [О} Отдельные представители. Акриловая (пропеновая) кислота СН2=СН - СООН представляет собой жидкость с резким запахом, смешивается с водой во всех отношениях. Широко используется для получения различных полимеров. Олеиновая кислота С8Н,7СН=СН - (СН^-СООН содержится в виде глидеридов в большинстве растительных масел и животных жиров, получается их гидролизом, представляет собой бесцветную маслянистую жидкость, легко окисляющуюся на воздухе, растворимую в органических растворителях и несме-шивающуюся с водой. Используется для производства парфюмерных и косметических средств, пеноочистителей, смачивателей и пластификаторов. Линолевая кислота СН3 - (СН2)3 - (СН2 - СН - СН)2 - (СН2)7 -- СООН. Содержится в виде глицеридов в растительных маслах, получается их гидролизом, представляет собой светло-желтую жидкость, хорошо растворимую в органических растворителях и нерастворимую в воде. Легко окисляется и полимеризуется на воздухе. Линоленовая кислота - маслянистая жидкость светло-желтого цвета, нерастворимая в воде и хорошо растворимая в органических растворителях. Содержится в виде глицеридов в растительных маслах и получается в результате их гидролиза. Легко окисляется и полимеризуется. Линолевая и линоленовая кислоты в организме человека и животных не синтезируются, но необходимы для жизнедеятельности, в организм поступают с пищей, поэтому они относятся к так называемым незаменимым жирным кислотам.
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Число карбоксильных групп характеризует основность кислоты.
В зависимости от количества карбоксильных групп карбоновые кислоты подразделяются на одноосновные карбоновые кислоты (содержат одну карбоксильную группу), двухосновные (содержат две карбоксильные группы) и многоосновные кислоты.
В зависимости от вида радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные, непредельные и ароматические. Предельные и непредельные кислоты объединяют под общим названием кислоты алифатического или жирного ряда.
Одноосновные карбоновые кислоты
1.1 Гомологический ряд и номенклатура
Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты

Формула гомологического ряда
Номенклатура ИЮПАК разрешает сохранять для многих кислот их тривиальные названия, которые обычно указывают на природный источник, из которого была выделена та или иная кислота, например, муравьиная, уксусная, масляная, валериановая и т.д.
Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н-СООН называется метановой кислотой, уксусная кислота СН 3 -СООН - этановой кислотой и т. д.
Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:

При составлении названий кислот с разветвленной цепью по рациональной номенклатуре их рассматривают как производные уксусной кислоты, в молекуле которой атомы водорода замещены радикалами, например, триметилуксусная кислота (СН 3) 3 С – СООН.
1.2 Физические свойства карбоновых кислот
Только с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства.
Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:
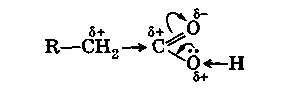
Следствием этого является значительное ослабление связи О-Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н +). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С-С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты.
Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами:
Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты - 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью.
Для большинства одноосновных карбоновых кислот рК а = 4,8, только муравьиная кислота имеет меньшую величину рК а (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп.
В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:

Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:

Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона.
Первые четыре представителя ряда карбоновых кислот - подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), - маслянистые жидкости, растворимость их в воде невелика.
Высшие кислоты (от С 10) - твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются.
Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.

На
физических свойствах карбоновых кислот
сказывается значительная степень
ассоциации вследствие образования
водородных связей. Кислоты образуют
прочные водородные связи, так как
связи О-Н в них сильно поляризованы.
Кроме того, карбоновые кислоты способны
образовывать водородные связи с участием
атома кислорода карбонильного
диполя, обладающего значительной
электроотрицательностью. Действительно,
в твердом и жидком состоянии карбоновые
кислоты существуют в основном в виде
циклических димеров:
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях.
Карбоновыми кислотами называются производные углеводородов, в молекуле которых содержится одна или несколько карбоксильных групп -COOH.
Общая формула карбоновых кислот:
В зависимости от природы радикала, связанного с карбоксильной группой, кислоты подразделяются на предельные, непредельные и ароматические.
Число карбоксильных групп определяет основность кислот.
Общая формула предельных одноосновных кислот: СnH2n+1COOH (или СnH2nO2).
Номенклатура. Распространены тривиальные названия. По правилам IUPAC к названию углеводорода добавляют "-овая кислота".
Изомерия.
1. Для алифатических кислот - изомеризация углеводородного радикала.
2. Для ароматических - изомерия положения заместителя при бензольном кольце.
3. Межклассовая изомерия со сложными эфирами (например, CH3COOH и HCOOCH3).
Таблица. Основные карбоновые кислоты (номенклатура, физические свойства)
|
Название |
Формула
|
tпл. |
tкип. |
r |
Раство- римость (г/100мл H 2 O ;25 °C) |
Ka
|
||
|
кислоты |
её соли
(эфиры) |
|||||||
| муравьиная | метановая | формиат | HCOOH |
100,5 |
1,22 |
1,77 . 10 -4 |
||
| уксусная | этановая | ацетат | CH 3 COOH |
16,8 |
1,05 |
1,7 . 10 -5 |
||
| пропионовая | пропановая | пропионат | CH 3 CH 2 COOH |
0,99 |
1,64 . 10 -5 |
|||
| масляная | бутановая | бутират | CH 3 (CH 2 ) 2 COOH |
0,96 |
1,54 . 10 -5 |
|||
| валериановая | пентановая | валерат | CH 3 (CH 2 ) 3 COOH |
0,94 |
4,97 |
1,52 . 10 -5 |
||
| капроновая | гексановая | гексанат | CH 3 (CH 2 ) 4 COOH |
0,93 |
1,08 |
1,43 . 10 -5 |
||
| каприловая | октановая | октаноат | CH 3 (CH 2 ) 6 COOH |
0,91 |
0,07 |
1,28 . 10 -5 |
||
| каприновая | декановая | деканоат | CH 3 (CH 2 ) 8 COOH |
0,89 |
0,015 |
1,43 . 10 -5 |
||
| акриловая | пропеновая | акрилат | CH 2 =CH-COOH |
1,05 |
||||
| бензойная | бензойная | бензоат | C 6 H 5 COOH |
1,27 |
0,34 |
1,43 . 10 -5 |
||
| щавелевая | этандиовая | оксалат | COOH I COOH |
189,5
|
1,65 |
K
1
=5,9
.
10
-2
|
||
| пальмитиновая | гексадекановая | пальмитат | CH 3 (CH 2 ) 14 COOH |
219
|
0,0007 |
3,46 . 10 -7 |
||
| стеариновая | октадекановая | стеарат | CH 3 (CH 2 ) 16 COOH |
0,0003 |
||||
Получение
1. Окисление первичных спиртов и альдегидов (кислородом на катализаторе; KMnO4; K2Cr2O7):
-[O]® R-
- C
OH
первичный
спирт
альдегид
2. Промышленный синтез муравьиной кислоты:
a) каталитическое окисление метана
2CH4 + 3O2 --t°® 2H-COOH + 2H2O
B) нагреванием оксида углерода (II) c гидроксидом натрия
CO + NaOH --p;200°C® H-COONa --H2SO4® H-COOH
3. Промышленный синтез уксусной кислоты:
a) каталитическое окисление бутана
2CH3-CH2-CH2-CH3 + 5O2 --t°® 4CH3COOH + 2H2O
B) нагреванием смеси оксида углерода (II) и метанола на катализаторе под давлением
CH3OH + CO ® CH3COOH
4. Ароматические кислоты синтезируют окислением гомологов бензола:
5 + 6KMnO4 + 9H2SO4 --t°® 5 + K2SO4 + 6MnSO4 + 14H2O
5. Гидролиз функциональных производных (сложных эфиров, ангидридов, галогенангидридов, амидов).
Химические свойства
1. Из-за смещения электронной плотности от гидроксильной группы O-H к сильно поляризованной карбонильной группе C=O молекулы карбоновых кислот способны к электролитической диссоциации:
R-COOH « R-COO- + H+
Сила карбоновых кислот в водном растворе невелика.
2. Карбоновые кислоты обладают свойствами, характерными для минеральных кислот. Они реагируют с активными металлами, основными оксидами, основаниями, солями слабых кислот.
2СH3COOH + Mg ® (CH3COO)2Mg + H2-
2СH3COOH + СaO ® (CH3COO)2Ca + H2O
H-COOH + NaOH ® H-COONa + H2O
2СH3CH2COOH + Na2CO3 ® 2CH3CH2COONa + H2O + CO2-
СH3CH2COOH + NaHCO3 ® CH3CH2COONa + H2O + CO2-
Карбоновые кислоты слабее многих сильных минеральных кислот (HCl, H2SO4 и т.д.) и поэтому вытесняются ими из солей:
СH3COONa + H2SO4(конц.) --t°® CH3COOH + NaHSO4
3. Образование функциональных производных:
a) при взаимодействии со спиртами (в присутствии концентрированной H2SO4) образуются сложные эфиры. Образование сложных эфиров при взаимодействии кислоты и спирта в присутствии минеральных кислот называется реакцией этерификации (ester с латинского "эфир").
Данную реакцию рассмотрим на примере образования метилового эфира уксусной кислоты из уксусной кислоты и метилового спирта:
CH3--OH(уксусная кислота) + HO-CH3(метиловый спирт) ®
® CH3--OCH3(метиловый эфир уксусной кислоты) + H2O
Общая формула сложных эфиров R--OR’ где R и R" - углеводородные радикалы: в сложных эфирах муравьиной кислоты - формиатах -R=H.
Обратной реакцией является гидролиз (омыление) сложного эфира:
CH3--OCH3 + HO-H ® CH3--OH + CH3OH
Как видно, процесс этерификации обратимый:
CH3--OH + HO-CH3 « CH3--OCH3 + H2O
Поэтому при наступлении химического равновесия в реакционной смеси будут находиться как исходные, так и конечные вещества.
Катализатор (ионы водорода) - одинаково ускоряют прямую и обратную реакции, то есть достижение равновесия. Чтобы сдвинуть равновесие в сторону образования эфира, следует брать в избытке исходные кислоту или спирт, или удалять один из продуктов реакции из сферы взаимодействия - например, отгоняя эфир или связывая воду водоотнимающими средствами.
Методом "меченых атомов" с помощью тяжёлого изотопа кислорода показано, что вода при этерификации образуется за счёт атома водорода спирта и гидроксила кислоты:
O-R’ --H+® R-
Учитывая этот факт, предложен следующий механизм реакции этерификации.
Кислород карбонильной группы кислоты захватывает протон, образуя оксониевый катион (I), который находится в равновесии с карбкатионом (II).
Молекула спирта атакует далее карбкатион (II), присоединяется к нему за счёт неподелённой пары электронов кислородного атома и образует оксониевый катион (III), который находится в равновесии с оксониевым катионом (IV).
От катиона (IV) отщепляется молекула воды, в результате чего образуется карбкатион (V), который находится в равновесии с оксониевым катионом (VI).
Оксониевый катион (VI) выбрасывает протон, являющийся катализатором реакции, приводя к молекуле конечного продукта - сложному эфиру.
b) при воздействии водоотнимающих реагентов в результате межмолекулярной дегидратации образуются ангидриды
CH3--OH + H-O--CH3 --(P2O5)® CH3--O--CH3 + H2O
C) при обработке карбоновых кислот пятихлористым фосфором получают хлорангидриды
CH3--OH + PCl5 ® CH3--Cl + POCl3 + HCl
Гидролиз всех функциональных производных карбоновых кислот (ангидридов, хлорангидридов, сложных эфиров и др.) приводит в кислой среде к исходным карбоновым кислотам, а в щелочной среде - к их солям.
4. Галогенирование. При действии галогенов (в присутствии красного фосфора) образуются a-галогензамещённые кислоты:
A
CH3-CH2-COOH --Br2;(P)® CH3- CH-COOH(a-бромпропионовая кислота(2-бромпропановая кислота)) + HBr
I
Br
A- Галогензамещённые кислоты - более сильные кислоты, чем карбоновые, за счёт -I эффекта атома галогена.
Применение
Муравьиная кислота - в медицине, в пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя.
Уксусная кислота - в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров).
Масляная кислота - для получения ароматизирующих добавок, пластификаторов и флотореагентов.
Щавелевая кислота - в металлургической промышленности (удаление окалины).
Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH - в качестве поверхностно-активных веществ, смазочных материалов в металлообработке.
Олеиновая кислота C17H33COOH - флотореагент и собиратель при обогащении руд цветных металлов.
КАРБОНОВЫЕ КИСЛОТЫ
Главной составной частью растительных и животных жиров являются сложные эфиры глицерина и высших жирных кислот (предельных - C15H31COOH пальмитиновой, C17H35COOH - стеариновой; непредельных C17H33COOH - олеиновой; C17H31COOH - линолевой; C17H29COOH - линоленовой).
O
II
CH2-O-
C-R
| O
II
CH-O- C-R’
| O
II
CH2-O- C-R’’
Физические свойства
Жиры, образованные предельными кислотами - твёрдые вещества, а непредельными - жидкие. Все жиры очень плохо растворимы в воде.
Первый синтез жира осуществил Бертло (1854 г.) при нагревании глицерина и стеариновой кислоты:
O
II
CH2-O
H HO-
C-C17H35
CH2-O-
C-C17H35
|
|
| O
II
CH-O
H + HO- C-C17H35
-®
CH-O-
C-C17H35 + 3H2O
|
|
| O
II
CH2-O
H HO- C-C17H35
CH2-O-
C-C17H35
Тристеарин
Химические свойства
1. Гидролиз (омыление) в кислой или в щелочной среде, или под действием ферментов:
В щелочной среде образуются мыла - соли высших жирных кислот (натриевые - твёрдые, калиевые - жидкие).
Все загрязнения гидрофобны, вода их плохо смачивает, поэтому стирать в чистой воде малоэффективно. Молекула кислотного остатка состоит из двух частей: радикала R, который выталкивается водой, и группы -COO-, которая полярна, гидрофильна и легко прилипает к частицам загрязнения. В мыльном растворе вода, выталкивая из своей среды углеводородные радикалы удаляет вместе с ними и группу -СОО-, которая адсорбирована на поверхности загрязняющей частицы, и тем самым загрязнение удаляется вместе с кислотным остатком.
Обычное мыло плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы кальция и магния дают с высшими кислотами нерастворимые в воде соли:
2RCOO- + Ca ® (RCOO)2Ca¯
В современных моющих средствах часто используют натриевые соли высших алкилсульфокислот, которые не связываются ионами Ca в нерастворимые соли.
2. Гидрирование (гидрогенизация) - процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира. При этом остатки непредельных кислот переходят в остатки предельных, и жидкие растительные жиры превращаются в твёрдые (маргарин).
3. Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее сколько г йода может присоединиться по двойным связям к 100 г жира.
При контакте с воздухом происходит прогоркание жиров, в основе которого лежит окисление по двойным связям (образуются альдегиды и кислоты с короткой цепью) и гидролиз под действием микроорганизмов.
Неспелые фрукты, щавель, барбарис, клюква, лимон… Что общего между ними? даже дошкольник, не задумываясь, ответит: они кислые. А вот обусловлен кислый вкус плодов и листьев многих растений различными карбоновыми кислотами - веществами, в состав которых входит одна или несколько карбоксильных групп -СООН.
У древних греков представление о кислом вкусе связывалось, прежде всего, с уксусом - раствором уксусной кислоты, образующейся при скисании вина. Само слово «уксус», или, как говорили жители Эллады, «оксис», означало «кислый». Получение уксуса при сухой перегонке - нагревании без доступа воздуха - древесины описано в сочинениях Иоганна Глаубера и Роберта Бойля. Однако природа этого вещества вплоть до XIX в. оставалась неизвестной. Алхимики считали, что при брожении вина винный спирт превращается в уксус, принимая на себя частицы - винного камня (гидротартрата калия С 4 H 5 О 6 K). Ещё в ХVIII в. брожение объясняли соединением кислых и горючих начал вина. Лишь в 1814 г. Якоб Берцелиус определил состав уксусной кислоты - С 2 Н 4 О 2 , а в 1845 г. немецкий химик Адольф Вильгельм Герман Кольбе (1818- 1884) осуществил полный её синтез из угля.
 А. Г. Кольбе
А. Г. Кольбе
Уксусная кислота относится к гомологическому ряду одноосновных карбоновых кислот. Низшие члены ряда при комнатной температуре представляют собой бесцветные жидкости с резким запахом. Простейшую из них - муравьиную кислоту НСООН, впервые получил в 1670 г. английский естествоиспытатель Джон Рей, нагревая муравьев в перегонной колбе. В природе широко распространены и более сложные по составу кислоты. Такова, например, масляная кислота СН 3 (СН 2) 2 СООН, которая образуется при прогоркании сливочного масла - это из-за нее испорченное масло так неприятно пахнет и горчит. Она обусловливает и запах пота. Родственная ей капроновая кислота СН 3 (СН 2) 4 СООН входит в состав козьего масла. В корнях растения валерианы содержится некоторое количество изовалериановой кислоты(СН 3) 2 СН – СН 2 СООН- ее можно выделить, обработав высушенные корни растения перегретым водяным паром.
Высшие кислоты, например стеариновая СН 3 (СН 2) 16 СООН и пальмитиновая CН 3 (CH 2) 14 COOH, впервые выделенная из пальмового масла, представляют собой бесцветные твёрдые вещества, не растворимые в воде. Долгое время основным их источником были природные жиры, например свиное сало или говяжий жир. Сейчас эти получают и синтетически - каталитическим окислением углеводородов нефти. Практическое значение имеют главным образом натриевые соли этих кислот - стеарат натрия C 17 H 35 COONa и пальмитат натрия C 15 H 31 COONa: они являются основными компонентами мыла.
В щавеле, а также в ревене, кислице, шпинате содержится щавелевая кислота НООС-СООН. Эта простейшая двухосновная кислота продукт распада некоторых аминокислот, например глицина. При нарушениях обмена веществ (в частности, при недостатке витамина В 12) в организме человека откладывается её малорастворимая кальциевая соль - оксалат кальция, это и есть так называемое оксалатное отложение солей. Янтарная кислота НООС-СН 2 СН 2 – СООН впервые была выделена алхимиками. Ещё Агрикола наблюдал при прокаливании янтаря образование похожего на соль белого налета янтарной кислоты (лат sal succini volatile - «летучая янтарная соль»).
Многие карбоновые кислоты — например, яблочная, винная, лимонная, хинная - образуются в вакуолях клеток плодов при частичном окислении глюкозы и в результате некоторых других биохимических процессов. Плоды цитрусовых богаты лимонной кислотой: в мякоти апельсина её около 2%, в грейпфруте - до 3%, а в лимоне - 6%. Поэтому неудивительно, что впервые она была выделена Шееле в 1784 г. именно из лимонов. Подобный эксперимент можно проделать и в школьной лаборатории: нужно лимонный сок обработать известью, а продукт этой реакции - кальциевую соль отфильтровать и разложить серной кислотой. Образующаяся в результате лимонная кислота переходит в раствор, который упаривают до начала кристаллизации. В зелёных яблоках, крыжовнике, плодах рябины содержатся не только яблочная, хинная, но и другие органические кислоты.
По основности кислоты делятся на:
Одноосновные (монокарбоновые), m = 1;
Двухосновные (дикарбоновые), m = 2;
Трехосновные (трикарбоновые), m = 3 и т. д.
Примерами дикарбоновых кислот являются:
В зависимости от строения углеводородного радикала R карбоновые кислоты делятся на:
Предельные (насыщенные), R = алкил;
Непредельные (ненасыщенные) - производные непредельных УВ;
Ароматические - производные ароматических УВ.
Насыщенные монокарбоновые кислоты
Наибольшее значение имеют насыщенные монокарбоновые кислоты, их общая формула:
Важнейшие представители гомологического ряда этих кислот представлены в таблице. В этой таблице приведены названия кислот RCOOH и кислотных остатков RCOO-.
В структуре карбоновых кислот часто выделяют также кислотные радикалы , или ацилы . Названия некоторых ацилов:

Номенклатура и изомерия
По международной заместительной номенклатуре название кислоты производят от названия соответствующего (с тем же числом атомов углерода) углеводорода с добавлением окончания -овая и слова кислота. Нумерацию цепи всегда начинают с атома углерода карбоксильной группы, поэтому в названиях положение группы -СООН не указывают. Например:
При составлении названий кислот, имеющих сложное строение, иногда также используют тривиальные названия кислот, соответствующие наиболее длинной прямой цепи. В этом случае атомы углерода в прямой цепи обозначают греческими буквами, начиная с атома , соседнего с карбоксильной группой: α (альфа),β (бета), γ (гамма), δ (дельта) и т. д., например:
Внутри класса предельных монокарбоновых кислот возможна только изомерия углеродной цепи. Первые три члена гомологического ряда (НСООН, СН 3 СООН, С 2 Н 5 СООН) изомеров не имеют. Четвертый член ряда существует в виде двух изомеров:
Пятый член ряда существует в виде четырех изомеров:
Монокарбоновые кислоты изомерны сложным эфирам карбоновых кислот:
Физические свойства

В твердом и жидком состояниях молекулы насыщенных монокарбоновых кислот димеризуются в результате образования между ними водородных связей:
Водородная связь в кислотах сильнее, чем в , поэтому температуры кипения кислот больше температур кипения соответствующих спиртов.
В водных растворах кислоты образуют линейные димеры:

Химические свойства
Для насыщенных монокарбоновых кислот характерна высокая реакционная способность. Это определяется главным образом реакциями карбоксильной группы (разрыв связей О-Н и С-О), а также реакциями замещения атомов «Н» у α-углеродного атома:

Реакции с разрывом связи О-Н (кислотные свойства, обусловленные подвижностью атома водорода карбоксильной группы)
Предельные монокарбоновые кислоты обладают всеми свойствами обычных кислот.
1.Диссоциация
В водных растворах монокарбоновые кислоты ведут себя как одноосновные кислоты: происходит их ионизация с образованием иона водорода и карбоксилат-иона:
Карбоксилат-ион построен симметрично, отрицательный заряд делокализован между атомами кислорода карбоксильной группы:
Делокализация стабилизирует карбоксилат-ион.
Карбоновые кислоты являются слабыми кислотами. Наиболее сильной в гомологическом ряду насыщенных кислот является муравьиная кислота, в которой группа -СООН связана с атомом . Алкильные радикалы в молекулах следующих членов гомологического ряда обладают положительным индукционным эффектом (+1) и уменьшают положительный заряд на атоме углерода карбоксильной группы. Это в свою очередь ослабляет полярность связи О-Н и тем в большей степени, чем больше УВ радикал. Поэтому в гомологическом ряду кислот их сила уменьшается с ростом числа атомов углерода в молекуле:
2.Образование солей:
а) взаимодействие с активными :
2НСООН + Mg → (HCOO) 2 Mg + H 2
2CH 3 COOH + CaO → (CH 3 COO) 2 Ca + H 2 O
CH 3 COOH + NH 3 → CH 3 COONH 4
CH 3 COOH + NH 4 OH → CH 3 COONH 4 + H 2 O
д) взаимодействие с солями более слабых кислот (карбонатами и гидрокарбонатами):
2CH 3 COOH + Na 2 CO 3 → 2CH 3 COONa + CO 2 + H 2 O
CH 3 CH 2 CH 2 COOH + NaHCO 3 → CH 3 CH 2 CH 2 COONa + CO 2 + H 2 O
II . Реакции с разрывом связи С-О (замещение ОН-группы)
Скачать рефераты по другим темам можно